Umí ocet opravit poškozenou DNA?
Ocet / octan / acetát vzniká ve zdravém organizmu jako hlavní produkt metabolizmu střevních bakterií v tlustém střevě. Odtud se dostává do celého těla krevním oběhem. Již několikrát jsem tady zmínil jeho pozitivní účinky na metabolizmus tuků, sacharidů nebo třeba podpůrných buněk nervového systému. Ale dnes to bude kalibr nejvyšší. Může acetát spustit opravu naší poškozené DNA? Tedy předejít rakovině? Na první pohled se to zdá být nesmysl. Taková obyčejná věc jako ocet nebo octan sodný? To už by se přece dávno vědělo, ne?
Jak vypadá DNA dnes ví asi každý. Jsou to dvě vlákna stočená do šroubovice. Informace uložená v DNA je tedy redundantní, každé vlákno obsahuje kompletní informaci. Pokud je nějak jedno vlákno poškozeno, např. radiací, druhé vlákno na přesně stejném místě obsahuje informaci, podle které lze první poškozené vlákno opravit.
Lehké opravitelné poškození vyvolává buněčnou senescenci. Zastaví se buněčné dělení. Je to logické, protože při buněčném dělení dojde k rozpletení jednotlivých vláken DNA a pokud je jedno vlákno poškozené, chyba by už nešla opravit. Tomuto stavu, kdy se buňka přestane dělit, říkáme buněčná senescence. Buňka také v tomto stavu změní metabolizmus tak, že omezí oxidační fosforylaci a preferuje fermentaci, tedy anaerobní metabolizmus. Je to z důvodu ochrany DNA, vzniká mnohem méně vysoce reaktivních látek, které by DNA dále poškozovaly. Buňka čeká na spuštění programu opravy DNA.
Tvrdí se, že stav buněčné senescence je trvalý. Co ji způsobuje? Už jsem zde uváděl studii, ve které autoři zajistili, že butyrát (krátká mastná kyselina produkovaná některými střevními bakteriemi, může výrazně zvýšit senescenci buněk střevního epitelu a může způsobit rakovinu. Jiná nedávná studie dokonce tvrdí, že spalování jakéhokoli tuku způsobuje senescenci buněk. Myslím, že toto odvážné tvrzení nebere v úvahu další významné faktory.
Jak jsme si totiž ukázali v předchozím příspěvku, nemusí při spalování tuků vůbec dojít k senescenci, bude-li správně spuštěno mitochondriální rozpojení (uncoupling). To autoři vůbec nezmiňují, hlavní úlohu zde hraje složení membrán a obsah oxilipinů v nich, jejich původ. Pokud jsou v membráně oxilipiny aktivující faktor PPARγ, pak dojde k senescenci. Pokud ale nedojde k aktivaci PPARγ nebo pokud budou účinky PPARγ zablokovány jiným způsobem (blokací HIF1, flavonoly jako třeba kvercetinem, myricetinem apod.), senescence se nespustí.
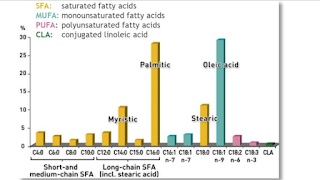
Některé oxilipiny uvolněné z membrán mohou i poškozovat DNA. Zejména produkty autooxidace arachidonové kyseliny, která se do membrány dostává prodloužením linolové kyseliny omega-6. Vysoký obsah některých rostlinných olejů ve stravě postupně plní buněčné membrány arachidonovou kyselinou, která odtamtud vytlačuje olejovou kyselinu, která není vůbec náchylná k autooxidaci. Tak se zdravé a odolné buněčné a mitochondriální membrány stávají zranitelnými a nemocnými. Při spalování tuků se tyto zoxidované produkty uvolňují a slouží jako signalizace, než jsou spáleny. Mohou i lehce poškodit DNA, což spustí ochranu DNA buněčnou senescencí. Aktivace mitochondriálního rozpojení pravděpodobně spálí tyto produkty ještě dříve, než by mohlo dojít k poškození DNA. Senescence se nespustí.
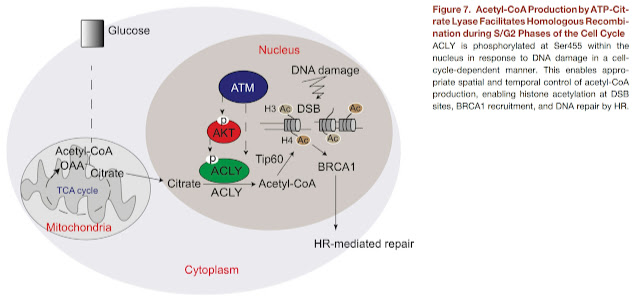
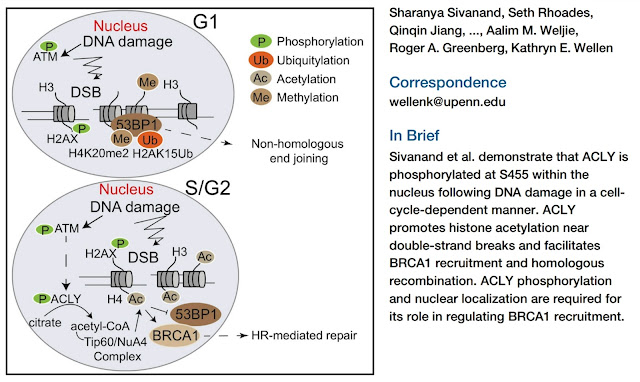
A nyní se dostaneme k tomu, jak se spouští proces opravy lehce poškozené DNA. Bude nám k tomu sloužit studie, ve které autoři zkoumali procesy kolem cytosolické molekuly acetyl-CoA. Já už jsem se zde také zabýval záhadou chybějící cytosolické molekuly acetyl-CoA, podívejte se na starší příspěvek. Nedostatečná hladina acetyl-CoA v buněčném cytosolu a buněčném jádru je obvykle následek spuštění de novo lipogeneze, tedy tvorby nových tuků, zejména v buňkách, které to dělat nemají. Prolínají se nám tu stavy pseudohypoxie, aktivované stabilizací transkripčního faktoru HIF1A, a buněčné senescence, aktivované poškozením DNA. Co je důležité, senescence aktivuje fosforylaci enzymu ACLY který zpracovává cytosolický a jaderný citrát na acetyl-CoA. Ten pak acetyluje v buněčném jádru hystony a spouští proces opravy DNA. My už víme, že acetát umí provést to samé. Nemám sice přímý důkaz, jen to, že acetát skvěle působí proti senescencí vyvolané inzulínové rezistenci a obezitě. Jestli v tomto účinku hraje roli i oprava poškozené DNA, to budou muset zjistit nějaké budoucí studie. Jeví se mi ale velice pravděpodobné, že část účinků bude právě účinek odstranění senescentních buněk buď opravou DNA, autofagií nebo apoptózou.
Nedostatek acetátu přirozeného původu v současné chemizované době plné antimikrobiálních konzervačních prostředků nás vede k tomu, že bychom ocet nebo čistý potravinářský octan sodný měli pravidelně doplňovat ve stravě. Doba metabolizmu octa je velmi krátká, cca 1 hodinu. Pokud tedy chceme doplnit přirozený acetát ze střevních bakterií, mělo by to být v nízké koncentraci a velmi často. Navrhuji tedy zředěný max. 1% roztok kyseliny octové cca 10-krát denně 50 ml nebo 10-krát denně cca 1 gram hydratovaného potravinářského octanu sodného. Pěkně rozložit užívání rovnoměrně přes celý den. Jde o to, aby acetát byl k dispozici tam, kde je potřeba a v čase, kdy je potřeba. To si řídí tělo samo. Úlohu v tom hraje zřejmě i laktát, který vpouští acetát do buněk transportéry MCT1.
Je třeba si uvědomit, že octan sodný je sůl obsahující sodík, tedy něco jako kuchyňská sůl. Může zvyšovat krevní tlak a mít jiné negativní projevy. Ředěný ocet se tedy může jevit jako vhodnější i když studie na hlodavcích používají octan sodný zcela běžně a látka je povolena pro potravinářské použití.
Zdroje:
Mitochondrial fatty acid oxidation drives senescence
Nuclear Acetyl-CoA Production by ACLY Promotes Homologous Recombination
DNA damage by lipid peroxidation products: implications in cancer, inflammation and autoimmunity


Komentáře
Okomentovat