Může čpavek z glutaminu za to, že tloustneme?
Když si shrneme základní studie, kdy na tučné stravě myši zůstaly hubené nebo dokonce zhubly již nasbíraný tuk, vyjde nám, že účinné je toto:
- Geneticky vypnutý transkripční faktor HIF-1α, tedy vypnutí (pseudo)hypoxie
- Vysoký příjem flavonolů potlačujících HIF-1α, tedy vypnutí (pseudo)hypoxie
- Genetické vypnutí NADPH oxidázy NOX2, tedy zdroje superoxidu a peroxidu vodíku při (pseudo)hypoxii
- Označkování enzymu xantinoxidáza ubikvitinem a jeho odstranění, tedy odstranění největšího zdroje superoxidu a peroxidu vodíku při tučné stravě, tedy zabránění aktivace (pseudo)hypoxie
- Vypnutí UCP2 v beta buňkách pankreatu, tedy snížení hladiny inzulínu a snížení produkce H2O2, tedy zabránění spuštění (pseudo)hypoxie snížením vstupu glukózy do buněk
O co tu tedy jde? Některý proces nám spouští extrémně vysoké hladiny superoxidu a následně peroxidu vodíku, které vyvolají obranné změny v aktivaci genů. Zvláštní na tom je právě aktivace enzymu xantinoxidáza (XO), jehož výstupem je močovina. Musí to tedy nějak souviset s metabolizmem aminokyselin. No, nebudu vás napínat, myslím si, že tu jde o aktivaci metabolizmu glutaminu a glutamátu, kterou jsem popsal při analýze zde. Vyšlo mi, že spalování samotných sacharidů nebo samotného tuku nevyžaduje spalování bílkovin (aminokyselin). Ale pokud spalujeme obojí najednou, TCA cyklus musí do spalovacího procesu přibrat i aminokyseliny/bílkoviny glutamin nebo glutamát jako důsledek činnosti anti-transportérů zajišťujících průchod důležitých molekul přes membrány.
Při oxidační deaminaci glutamátu v mitochondrii se uvolňuje čpavek. K tomu dochází právě při normálním běhu TCA cyklu, proto se mi zdá, že pokud navýšíme množství zpracovaného glutamátu současným spalováním sacharidů a tuků, zvýší se i otrava čpavkem a buňka na to musí reagovat. Aktivuje transkripční faktor HIF-1α a přejde na transaminaci, sníží se produkce čpavku, ale zároveň se i otočí běh části TCA cyklu do protisměru a tuky se budou tvořit z aminokyselin. Neprobíhá to na všech buňkách zároveň, pouze na některých. Většina buněk tak může déle pracovat normálně. Současné spalování sacharidů a tuků (při aktivované lipogenezi DNL viz dále) tedy zvyšuje otravu mitochondrií čpavkem. Přepnutí metabolizmu na fermentaci glukózy je obranným mechanizmem snižujícím projevy otravy pro okolní buňky.
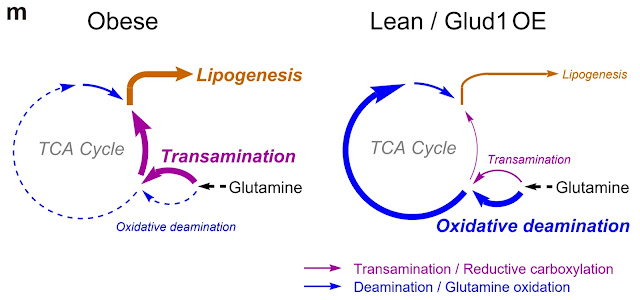 |
| Obese - cesta metabolizmu glutaminu směrem k ukládání tuku při aktivní lipogenezi (DNL), Lean - cesta metabolizmu glutaminu pokud se tuk neukládá. |
Toto ale neplatí v případě, když se nám podaří zabránit sacharidům ve spuštění tzv. de novo lipogeneze (DNL). Pokud nedojde ke spuštění DNL, bude vše v pořádku i při současném spalování sacharidů s tuky, nebudou se muset spalovat aminokyseliny v TCA cyklu. To je velice zajímavé a nadějné. Nebude tedy produkován jedovatý amoniak a nebude potřeba zachraňovat pH buňky aktivací (pseudo)hypoxie. Také zabráníme otočení části TCA cyklu a zpomalení metabolizmu. Navíc zřejmě zabráníme i aktivaci enzymu XO a tedy vzniku velkého množství superoxidu a močoviny. Jak vypneme DNL i při konzumaci sacharidů? Stačí aktivovat fosforylaci enzymu ACC1 pomocí enzymu AMPK. Fosforylace ACC1 zastaví tvorbu nových tuků z aminokyselin a tak napraví TCA cyklus pro oxidační fosforylaci.
Jak konkrétně to můžeme provést? Octem nebo octanem. Octan funguje! Našel jsem další studii, která potvrzuje, že octan by mohla být cesta. Tentokrát jako glycerol triacetát (trioctan glycerolu, triacetin, E1518).
O tom, že octan (acetát) dokáže opravit metabolizmus tak, že napraví obezitu myší a ty zhubnou na normální váhu, jsem zde již psal. Nyní máme další studii, která to potvrzuje. Co je důležité, víme i mechanizmus, jakým to funguje, z předchozí studie. A zřejmě to nemusí být pouze acetát ze stravy, mohl by to být i acetát vyrobený jaterními peroxizomy při metabolizmu omega-3 mastných kyselin., např. DHA z rybího tuku.
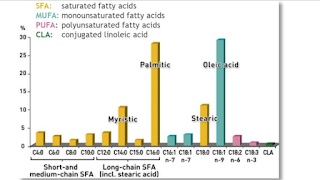
Laboratorní potkani byli nejprve rozděleni do dvou skupin a 8 týdnů krmeni kontrolní stravou nebo hodně tučnou stravou. Potom byla skupina na hodně tučné stravě rozdělena do tří skupin. Jedna pokračovala ve stejné tučné stravě, druhá dostala místo části tuků triacetin a třetí dostala místo části tuků MCT olej. Celkově se neměnilo procento kalorií z tuků. Výsledek vidíte na obrázku, nasazení triacetinu během jednoho týdne způsobilo obrovskou změnu v metabolizmu takovou, že tělesná hmotnost se snížila prakticky okamžitě na úroveň kontrolní skupiny. Nahrazení tuků MCT olejem sice také mělo vliv, ale pouze preventivní, MCT olej nedokázal zvrátit již narušený metabolizmus tuků. Zejména je vidět nárůst kalorické hodnoty přijímané stravy. Triacetin naopak způsobil okamžitě snížení kalorického příjmu, snížil hlad. Možná by bylo zajímavé spojení MCT a triacetinu, procentuální množství triacetinu bylo totiž v této studii velmi vysoké, 65% triacetinu v tuku. Obsah tuku ve stravě byl 46 % energetických, celkově tedy bylo triacetinu 30% energetických. Pro porovnání, studie na myších s octanem sodným používala 5% hmotnostních ve stravě, což by mohlo odpovídat celkovým cca 10 % energetickým, tedy 3x méně acetátu a fungovalo to velmi podobně.
Mechanizmus nám prozrazuje již předchozí studie. Pomocí fosforylace ACC1, tedy pomocí enzymu AMPK. Samotné zastavení procesu DNL by ale nestačilo. Efekt AMPK je daleko širší, dojde k obnovení hladiny cytosolického acetyl-CoA, ten acetyluje HIF-1α a vypne fermentaci a zastaví pseudohypoxii, tedy metabolizmus bez potřeby kyslíku. HIF-1 aktivuje NADPH oxidázu (NOX2) a je zdrojem superoxidu a peroxidu vodíku nezávislém na hladině inzulinu. Acetát tedy působí podobně jako genetické vypnutí HIF-1α. Dalším efektem je normalizace směru TCA cyklu, aminokyseliny (proteiny) se přestanou používat na tvorbu tuku, to sníží podstatně množství uvolněného jedovatého čpavku. Čpavek uvolňovaný při zpracování aminokyselin zastavuje činnost superoxid dismutázy SOD a vynucuje tak přechod na pseudohypoxii. Čpavek dále aktivuje enzym xantinoxidázu, která je dalším zdrojem superoxidu nezávislém na hladině inzulinu. Acetát tedy potlačí generování čpavku a generování superoxidu a peroxidu vodíku enzymem XO. Zastaví tvorbu ROS mimo mitochondrii. Všechny zdroje superoxidu a peroxidu vodíku, které nepocházejí z TCA cyklu nebo z elektronového transportního řetězce, narušují inzulinovou signalizaci a řízení metabolizmu inzulinem.
Může tedy za naše problémy s metabolizmem čpavek? Myslím si, že v mnoha případech ano.
Ještě pár obrázků, co způsobuje čpavek mitochondriím nervových buněk. Látka MK-801 blokuje NMDA receptor, blokace tohoto receptoru eliminuje negativní účinky čpavku.
 |
| Octan amonný snižuje aktivitu superoxid dismutázy, zvyšuje tedy hladinu superoxidu, ale snižuje hladinu peroxidu vodíku. |
 |
| Mn-SOD - superoxid dismutáza, Catalase - kataláza, GSH peroxidase - glutathion peroxidáza (hlavní antioxidant), Glutathione reductase - hlavní obnovovač redukovaného glutathionu. |
 |
| XO - xantinoxidáza, hlavní zdroj superoxidu při vystavení mitochondrie čpavku. Hlavní faktor zapínající metabolizmus tvorby tuku. |
 |
| Blokace NMDA receptoru eliminuje účinky čpavku na mitochondrie. Látka MK-801 vypnutím NMDA receptoru zesiluje účinky GLP-1 jako prostředku pro eliminaci metabolického syndromu. |
Zdroje:
Myricetin protects against diet-induced obesity
UCP2 KO mice exhibit ameliorated obesity and inflammation induced by high-fat diet feeding
Causes and Consequences of A Glutamine Induced Normoxic HIF1 Activity for the Tumor Metabolism
Novel role of xanthine oxidase-dependent H2O2 production in 12/15-lipoxygenase-mediated de novo lipogenesis, triglyceride biosynthesis and weight gainSources of oxygen radicals in brain in acute ammonia intoxication in vivo
GLP-1-directed NMDA receptor antagonism for obesity treatment




Komentáře
Okomentovat