Mohou MCT oleje snížit obsah omega-6 v membránách?
Už to určitě víte. Oxidační stres jakéhokoli druhu vyvolá aktivitu enzymů zvaných fosfolipázy, zejména iPLA2γ, která uvolňuje zoxidované polynenasycené tuky z mitochondriální membrány. Takto buňky sledují svůj stav, oxidační stres, a výsledné uvolněné a zoxidované produkty pocházející z linolové kyseliny omega-6 (LA/ARA, např. 4-HNE) slouží jako signál pro mnoho procesů. Např. i pro vyvolání chronického zánětu třeba tím, že aktivují aldóza reduktázu (AR) a polyolovou dráhu. Zvýšené hladiny glukózy (HG) se tak při nedostatečné funkci enzymu ALDH2 s přichycenými molekulami 4-HNE stanou problematickými, místo nápravy oxidačního stresu jej dále prohlubují. Chybějící aktivitu ALDH2 lze obnovit pomocí H2S (zde použit NaHS) nebo aktivací enzymu CSE (např. omezením methioninu a cysteinu ve stravě).
Mám o tom zde mnoho příspěvků, většinou se týkají jaterních buněk nebo buněk slinivky břišní, tedy i sekrece inzulínu. Ale pokud tuky uvolněné z membrán pocházejí z omega-3 mastných kyselin (DHA, EPA) nebo ještě lépe z mononenasycené olejové kyseliny (OA), reakce je jiná, není zánětlivá. Naším přáním tedy je, abychom měli v membránách více olejové kyseliny a méně linolové kyseliny. Ale jak to zařídit?
Z nadpisu asi tušíte, kam mířím, ano, co kdyby vyšší konzumace olejů se středně dlouhým řetězcem (MCT) dokázala část molekul arachidonové kyseliny omega-6 (ARA) usazených v membránových fosfolipidech nahradit molekulami bezpečné olejové kyseliny (OA)? To by bylo dobré, nemyslíte? Víme, že to umí nízkotučná sacharidová strava. Ale ta za situace zvýšené aktivity enzymu AR produkuje sorbitol a fruktózu. To nechcete! Co kdyby šlo dosáhnout podobného nahrazení molekul v membránách bezpečněji pomocí MCT oleje? Dokonce i v prostředí s aktivní aldózo reduktázou (AR)? No zatím nevím. Podívejme se na jednu starší studii, už jsem na ni kdysi dávno odkazoval.
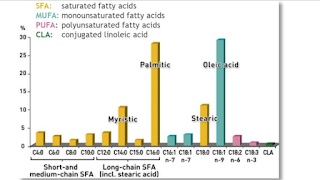
Jedná se o studii účinků stravy na zdravé muže, jimž bylo podáváno o 50 % více kalorií v jídle po dobu jednoho týdne a zkoumal se vliv tuků. Jídlo obsahovalo 40 % tuku ve dvou formách, buď jako LCT (long chain triglyceride), tuky obsahující hlavně olejovou C18:1 a linolovou kyselinu C18:2, nebo jako MCT (medium chain triglyceride), tedy tuky obsahující hlavně mastné kyseliny C8:0 a C10:0. MCT oleje se prodávají jako doplněk stravy, není problém je získat.
Ukažme si nejzajímavější obrázek, obsah volných mastných kyselin s délkou 18 až 20 uhlíků (C18-C20). Tuky vstupují do buněk ve formě volných mastných kyselin. Z předchozích příspěvků už víme, že indikátorem správného zpracování tuků je exkluzivně hladina neesterifikované olejové kyseliny. Ta řídí ukládání do tukové tkáně, export tuků z jater a přidávání tukových buněk diferenciací preadipocytů. Pak je dalším indikátorem hladina palmitové kyseliny C16, ale to už není regulační signál, to je signál nouzový, zvýšená hladina C16 znamená, něco je hodně špatně. Podívejme se teď na některé grafy ze studie.
Citace ze studie:
"Analysis of triglyceride fatty acids on the packed column revealed that C18:l was increased (32.1% vs 30.4%) while C18:2 was markedly decreased (8.3% vs 35.6 %) in MCT as compared to LCT feeding. Considering that fasting triglycerides were 2.5-fold higher when subjects were on MCT compared to when they consumed LCT diets, these data suggest that the absolute amounts of all triglyceride fatty acids except C18:2 and C20:4 were increased with MCT feeding. That is, in addition to an increase in triglyceride MCFAs (which were essentially absent from triglycerides during LCT feeding), 14:O increased approximately 6-fold, 16:O and 16:l increased approximately 4-fold, 18:O increased approximately 3-fold, and 18:l increased approximately 2.5-fold compared with LCT feeding."
„Analýza triglyceridových mastných kyselin ukázala, že C18:1 (OA) byl zvýšen (32,1 % oproti 30,4 %), zatímco C18:2 (LA) byl výrazně snížen (8,3 % oproti 35,6 %) v MCT ve srovnání se stravou LCT. Vzhledem k tomu, že triglyceridy nalačno byly 2,5krát vyšší, když subjekty konzumovaly MCT, ve srovnání s konzumací LCT stravy, tato data naznačují, že absolutní množství všech triglyceridových mastných kyselin kromě C18:2 (LA) a C20:4 (ARA) bylo při stravě MCT zvýšeno. To znamená, že kromě zvýšení triglyceridových MCFA (které v triglyceridech během stravy LCT v podstatě chyběly) se C14:0 zvýšil přibližně 6krát, C16:0 (PA) a C16:1 přibližně 4krát, C18:0 (SA) se zvýšil přibližně 3krát a C18:l (OA) přibližně 2,5krát ve srovnání se stravou LCT."
Konec citace
Shrňme si to, MCT oleje ze stravy jdou přímo do jater, kde navyšují hladinu molekul acetyl-CoA a spouští de novo lipogenezi (DNL), tedy tvorbu saturovaných a mononenasycených tuků. Mění tedy zásadně poměry mastných kyselin v triglyceridech. Produkují kyselinu palmitovou, ale ta je prodloužena a desaturována na kyselinu olejovou. A MCT oleje přitom neobsahují téměř žádnou linolovou kyselinu. Snižují tedy relativní zastoupení linolové a arachidonové kyseliny v triglyceridech, které játra posílají do těla k uložení nebo metabolizování na energii ATP. U této studie bylo pozorováno snížení relativního obsahu LA v triglyceridech o cca 75 % (ze 35 % na 8 %). To může být velmi zajímavé, pokud vaše vlastní zásoby tuku obsahují mnoho linolové a arachidonové kyseliny.
Promítne se tato změna i do fosfolipidů? No jak vidíme výše, v této krátkodobé studii moc ne. Hladina C18 se sice trochu snížila, ale jestli je to významné, to nevíme. Podle mne je největší změna navýšení o 30 % u C22:6, tedy DHA, dlouhé omega-3. To by mohlo být důležité, protože DHA omezuje vstup tuků do buňky potlačením CD36 a tak umožňuje současné zpracování tuků i sacharidů bez vyvolání metabolických problémů. Bylo by zajímavé pozorovat dlouhodobější vliv, jak se projeví výměna mastných kyselin ve fosfolipidech z dlouhodobého hlediska a bez přejídání. Na to tato studie odpověď nemá.
MCT oleje zvyšují okamžitý výdej energie teplem. Ten je obvykle spojený s nárůstem oxidativního stresu. V této studii to nezjišťovali, ale z jiných studií víme, že dlouhé polynenasycené tuky po nějakém čase snižují výdej energie teplem, zřejmě tím, jak peroxidují v oxidačním prostředí. Já to přisuzuji konkrétně účinkům 4-HNE na enzymy, na zpomalení jejich funkce, což vyvolá nedostatek molekul H2S a nedostatečnou S-sulfhydrataci enzymů. Mohly by MCT oleje ve stravě působit na obnovení tvorby H2S? Jedním z výsledných produktů metabolizmu sirných aminokyselin je pyruvát. Vysoké hladiny nezpracovaného pyruvátu tedy mohou blokovat tvorbu H2S. Pyruvát může být zpracován buď na laktát, acetyl-CoA nebo na oxaloacetát. Víme, že procesy tvorby nových tuků (DNL) a tvorby nové glukózy (GNG) se spouštějí společně např. prostřednictvím PPARα (spouští spalování tuků v peroxizomech, produkci H2O2 a acetátu), zvýšením produkce H2O2, tedy oxidativním stresem (obvykle H2O2) a olejovou kyselinou vytvořenou např. z acetátu/acetyl-CoA procesem DNL.
Balance mezi procesy DNL a GNG je velmi důležitá, vyšší hladina acetyl-CoA spouští GNG (enzym PC a spotřebovává pyruvát) a DNL odebírá acetyl-CoA, takže snadné ukládání tuků potlačí GNG, sníží hladinu glukózy. Obtížné a pomalé ukládání tuků zvýší hladinu acetyl-CoA a podpoří GNG a tvorbu glykogenu, někdy i glukózy. Zdá se, že vše je spojené se vším, aby se to regulovalo jako celek.
Je obtížné jednotlivé procesy od sebe separovat, může to snadno vést k zavádějícím závěrům a doporučením. MCT oleje svým rychlým metabolizmem zřejmě navyšují hladinu acetyl-CoA a spouští tak GNG i DNL. Ale mění i poměr mezi GNG a DNL. Pokud jsou v jídle výhradně krátké a střední mastné kyseliny bez dlouhých řetězců, připomíná to metabolicky nízkotučnou sacharidovou stravu. Aktivuje se DNL pro konverzi středních řetězců na olejovou kyselinu vhodnou k uložení. To je doplněno GNG až po G6P a tvorbou glykogenu. Zde do procesu vstupují cukry, glukóza a fruktóza. Zatímco fruktóza nepotlačuje glukoneogenezi, glukóza ano. Tím je kontrolováno množství stravy, které je potřeba sníst. Konzumace MCT tedy nevedou k přejídání, pokud není vypnuta glukoneogeneze. Tu lze vypnout pomocí PPARα, to jsme už viděli.
Co udělá vypnutí PPARα v játrech (Pparαhep-/-) anebo v celém organizmu (Pparα-/-)? Co se dá vyčíst ze studií?
Je zajímavé, že spojení mezi PPARα a GNG není obecně moc známo. Tak se stane, že autoři ve studii zkoumající právě tento faktor glukoneogenezi vůbec nezmiňují, vůbec ji nezkoumají. Vůbec!
Podívejte se na obrázku výše, jak se mění hladiny glukózy na lačno u myší s vypnutým PPARα pouze v játrech (červeně), v celém organizmu (modře) a bez vypnutí (šedě). Pro dva druhy stravy, standardní nízkotučnou (CTRL) a tučnou stravu se sádlem a cukrem D12492 (HFD). Tučná strava evidentně podporuje GNG už i u kontrolní skupiny (WT HFD). Když vypnete GNG v játrech, sníží se glukóza na lačno, když vypnete GNG v celém těle, glukóza se zcela normalizuje, překvapivě i při OGTT testu (AUC)! Vidíte to taky? V celé studii není nic o glukoneogenezi, i když zkoumali všechny geny a mastné kyseliny, všechny dráhy atd. Co je to v dnešní době za podivnou vědu? Já jsem laik, proč bych jim měl radit? (Doplnění: Jedná se konkrétně o vypnutí tvorby glukózy z glycerolu)
- Proč při standardní myší stravě vypnutí PPARα v játrech vede k nárůstu GNG v jiné části těla a zvýšení hladin glukózy?
- GNG v jiné části těla neprodukuje glykogen, zvedá proto krevní glukózu a sekreci inzulínu více než jaterní GNG?
- Proč dojde k navýšení syntézy cholesterolu?
- Došlo k navýšení lipolýzy tak, že bylo nutné spustit GNG v jiné části těla?
- Je syntéza cholesterolu řešením metabolických problémů souvisejících se sníženou GNG v játrech?
- Souvisí to s odbouráváním aminokyselin?
Zajímavé je, že žádnou z těchto otázek si autoři v této studii snad ani nepoložili. Nevíme proč, ani jaký jiný orgán musel nahradit jaterní GNG.
Glukoneogeneze ve stavu na lačno reguluje hladinu inzulínu a snižuje lipolýzu, uvolňování tuků z tukové tkáně. Předpokládám, že při vypnutí GNG v játrech dojde ke zvýšení hladiny např. olejové nebo linolové kyseliny a zvýší se tak GNG např. v ledvinách. Tím by se dala vysvětlit vyšší hladina krevní glukózy u skupiny CTRL Pparαhep-/-.
Ale proč ten vyšší cholesterol? Už jsem tu jeden takový příspěvek měl. Ten ukazoval, že nedostatek produktů TCA cyklu pro funkci malát-aspartátového cyklu vede při omezení mitochondriálního komplexu I k navýšení syntézy cholesterolu v játrech. Je to řešení problému, problému s exportem elektronů z mitochondrií. Je řešen zvýšenou produkcí a zvýšeným exportem cholesterolu z mitochondrií.
A co udělalo celkové vypnutí PPARα? Snížilo produkci nových tuků pomocí DNL? Snížilo se množství FFA, tedy volné olejové kyseliny v krvi? Řekl bych, že ano. Vypnutí GNG pak asi nevadí na standardní stravě, protože není zapnutá ani DNL v tukové tkáni, kterou ovládá olejová kyselina. Přesto se tuky velmi snadno ukládají, díky nízké inzulínové rezistenci tukové tkáně. Vše je spojené se vším.
Co říci závěrem?
Tuky se středním řetězcem (MCT) mohou být vhodným doplňkem stravy. V některých potravinách jsou zastoupeny poměrně hojně, např. v másle nebo kokosovém oleji. V jiných zcela chybí. V našem toxickém prostředí a vlivem autooxidace omega-6 olejů zřejmě dochází k nevyváženosti mezi tvorbou/ukládáním glykogenu a mezi tvorbou/ukládáním tuků. Dochází k nedostatečné S-sulfhydrataci enzymů (PC, ALDH2) a to způsobuje tuto nevyváženost mezi GNG a DNL. Mezi těmito procesy musí být spolupráce a soulad, jinak to vede k nerovnováze příjmu a ukládání stravy, k obezitě. Tak se mi to jeví. A právě tuky s krátkým a středním řetězcem, SCFA a MCT oleje, mohou přispět k obnovení této narušené rovnováhy tím, že podporují nejen novou tvorbu olejové kyseliny jako hlavního regulátoru ukládání tuků, ale i tvorbu glykogenu jako indikátoru množství snědeného jídla, což samotná olejová kyselina ani olivový olej neumí. Navíc pravděpodobně v delším časovém období dokáží nahradit polynenasycené tuky omega-6 v membránových fosfolipidech nově vytvořenou, bezpečnou a stabilní olejovou kyselinou.
Zdroje:
Changes in blood lipids during six days overfeeding with medium or long chain triglycerides
Hepatocyte-specific deletion of Pparα promotes NAFLD in the context of obesity
PPARα governs glycerol metabolism
.












Komentáře
Okomentovat