Je snížení cholesterolu rostlinnými oleji způsobeno právě jejich peroxidací?
Náhodou jsem se podíval na starší studii z roku 2004, která ukazuje, že oxidační stres ovlivňuje export tuků z jater ve formě částic VLDL. Představte si, že každá lipoproteinová částice VLDL/LDL obsahuje právě a pouze jednu molekulu proteinu ApoB100, takže jsou zcela nezbytné pro export tuků z jater. Máme tedy už tři nezbytné produkty, které potřebujeme pro zdárný export tuků z jater, t.j. olejovou kyselinu, H2O2 a ApoB100.
Olejovou kyselinu získáme z jídla nebo ze saturovaných tuků pomalým procesem DNL. Při relativně nízkotučné stravě to není žádný problém. Saturované tuky také při přebytku vytvoří dostatek H2O2 pro aktivaci enzymů syntetizujících VLDL.
Jak je to s ApoB100? Ten se také snadno vyrobí. Ale studie nám říká, že existuje systém, který kontroluje kvalitu exportovaných tuků v částicích VLDL. Pokud jsou přítomny peroxidované polynenasycené tuky, enzymatický systém PERPP odbourá molekuly ApoB100 a žádné částice VLDL nemohou být exportovány, omezí se tak export tuků z jater a zvýší se ukládání tuků v nich, tedy ztukovatění jater.
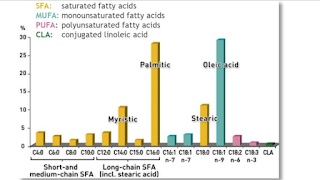
Závislost je nepřímo úměrná a je celkem lineární, čím více nenasycených vazeb, citlivých na peroxidaci, čím více peroxidovaných tuků (TBARS), tím nižší je výsledný počet použitelných molekul ApoB100, s několika výjimkami. Peroxidovaná linolová kyselina (LNA) odbourává ApoB100 nejrychleji a naopak nasycená kyselina myristová (MA, C14:0) nejpomaleji.
Je to zřejmě právě tento mechanizmus, kterým polynenasycené rostlinné oleje spolehlivě snižují hladinu cholesterolu LDL-C. Je to známý efekt, kterým lze v podstatě i sledovat množství polynenasycených olejů ve stravě ve studiích vlivu složení stravy.
Zde se opět dostáváme k problému, jestli je to dobře nebo špatně. Jestli nám to prospívá nebo škodí. Už to není tak jednoznačné, že? Pokud rostlinné oleje potlačují export tuků z jater, měli bychom se zajímat o to, jak snížíme množství tuků k exportu, aby se nám nehromadily v játrech. Normální reakcí je totiž zvednutí hladiny volných mastných kyselin v krvi. To aktivuje PPARα v játrech a PPARγ v tukové tkáni pro obnovení ukládání, pokud to nepomůže, vysoké FFA způsobí zvýšení glukoneogeneze, hladina glukózy na lačno se zvýší spolu s inzulínem, je to cesta k diabetu.
V játrech PPARα aktivuje beta oxidaci tuků, takže se zvýší hladiny acetyl-CoA a H2O2. Acetyl-CoA aktivuje enzym PC a glukoneogenezi (GNG). Je to celkem jednoduchá regulace. Pokud se daří tuky exportovat v částicích VLDL, snižuje se hladina acetyl-CoA a snižuje se tvorba nové glukózy a ta se více používá jako zdroj energie. Pokud export zarazíme, a to může nastat i neochotou tukové tkáně tuky přijímat, vyšší hladina FFA aktivuje prostřednictvím PPARα metabolizmus tuků v játrech a acetyl-CoA aktivuje tvorbu nové glukózy z glycerolu uvolněného z tukové tkáně. Přepínačem je vlastně jaterní hladina molekul acetyl-CoA a hladina volných mastných kyselin, která aktivuje transkripční faktory pro aktivaci produkce potřebných enzymů.
Takže, našli jsme právě souvislost, proč linolová kyselina tak mocně aktivuje PPARα i PPARγ? Protože blokuje export VLDL odstraněním potřebného ApoB100 vlivem své vlastní peroxidace? Je to výstupní kontrola kvality VLDL, která zamezí exportu peroxidovaných lipidů?
Moje hypotéza je prostě taková, že tuky uvolněné jako volné mastné kyseliny z tukové tkáně je potřeba okamžitě spálit nebo zase včas zabalit v játrech do VLDL částic. Pokud nějaké FFA zbydou v krvi, je to signál, že něco nefunguje úplně správně a podle toho, jaká konkrétní kyselina přebývá, tělo reaguje.
Pokud přebývá olejová kyselina (OA), sama aktivuje ukládání do triglyceridů a VLDL a následně do tukové tkáně. Aktivuje se PPARα i PPARγ. Nemusí se tedy ani spouštět DNL, pouze je třeba aktivovat GNG (víme, že bez OA se GNG nespustí), tedy enzym PC pomocí zvýšení acetyl-CoA, to umožní tvorbu triglyceridů. Jelikož se OA nespaluje příliš rychle, hladina acetyl-CoA se zvýší automaticky při přebytku.
Pokud srovnáme rychlosti spalování sojového (SO), olivového (OO) a kokosového (CO) oleje v jaterní buňce, pak vítězí polynenasycené tuky nad olivovým olejem a nejpomalejší je kokosový olej. Proč je kokosový olej nejpomalejší? Řekl bych, že se nejprve musí upravit část laurové kyseliny C12:0 prodloužením a desaturací na olejovou kyselinu C18:1. Nejde to tak rychle. Bez olejové kyseliny nic nefunguje. Olejová kyselina je optimální, ale polynenasycené tuky C18 jsou rychlejší!
Proč? Já myslím, že je to tím, že se zároveň spaluje i glukóza. Tyto tuky nevyvolávají dostatečné zpomalení glykolýzy. Je k dispozici příliš mnoho NAD+, který vzniká buď činností enzymu DECR nebo dalším prodlužováním a další desaturací PUFA. To vytváří neskutečné nároky na antioxidační systém a ten to vydrží jen omezenou dobu. Po vyčerpání antioxidační ochrany se začnou tvořit peroxidované PUFA aldehydy. Teprve potom dojde ke zpomalení jak beta oxidace a k omezení glykolýzy.
Podívejme se na studii, kterou jsem tu již jednou probíral. Nyní mám více poznatků a můžeme upřesnit komentář, jak se věci pravděpodobně odehrávají. Studie je zajímavá tím, že používá výše jmenované tři oleje ve dvou množstvích, 7 % a 21 %, čili máme k dispozici údaje pro šest diet. Navíc máme dvě genetické varianty myší lišící se expresí PPARα (WT, PPARα KO).
Nejzajímavější je olivový olej, který prakticky není deaktivací PPARα ovlivněný a poskytuje optimální výsledky i z hlediska zdraví střevní stěny a aktivace propouštění LPS do krevního oběhu.
Co dělá kokosový olej? Při nízké koncentraci a při vypnutém PPARα (tedy i vypnuté GNG) se chová dost podobně jako olivový olej, je to proto, že nízká koncentrace umožňuje dostatečnou tvorbu olejové kyseliny pomocí DNL. To se ovšem mění při vysokém obsahu, kdy nedostatečná úroveň olejové kyseliny omezuje export VLDL a ukládání tuku v tukové tkáni. Projeví se to jako hubený fenotyp. Musí se více spalovat ale více se zcela určitě ukládá i v játrech.
Pokud ale ponecháme PPARα funkční, kokosový olej ukládá poměrně dost tuků v tukové tkáni i při vysoké inzulínové rezistenci. Sice z jiných studií víme, že nezpůsobuje senescenci adipocytů. Ale aktivuje propustnost střeva pro endotoxiny. Spustí reakci podobnou bakteriální infekci. LPS aktivuje lipolýzu a rychlou transformaci středních mastných kyselin na dlouhé, vhodné pro uložení. Účinek endotoxinu LPS pravděpodobně probíhá prostřednictvím aktivace PPARα, zvýšením H2O2 a aktivací enzymu AR. Vypnutím PPARα se tento účinek silně potlačí. Propustnost střeva je v případě kokosového oleje zásadní, ale při bakteriální infekci může pomoci spustit obranné mechanismy.
Sojový olej v malém množství omezuje export VLDL a ukládání tuků. To aktivuje glukoneogenezi a snižuje příjem potravy. Antioxidační ochrana ještě funguje a není přetížena. Ale při vyšším množství PUFA ve stravě přestane antioxidační ochrana fungovat a vyprodukují se aldehydy 4-HNE a přilepí se na enzymy. Zastaví se jaterní GNG i export VLDL. Zvýší se volné mastné kyseliny a linolová kyselina se přímo ukládá v adipocytech do triglyceridů, protože PPARγ je aktivní. Omezená jaterní GNG ale neznamená, že je omezena tvorba glukózy např. v ledvinách, glukóza na lačno bude vysoká a nedostatečná rychlost jaterní produkce glykogenu bude kompenzována přejídáním. Ukládání přestane být řízeno játry. Ale nestane se to hned, pár týdnů potrvá, než se játra dostatečně poškodí.
Ukazuje se, že právě aktivace PPARα je velmi důležitým ochranným procesem při spalování polynenasycených tuků, hlavně při jejich malém množství ve stravě. Jednak aktivuje peroxizomy a doplňuje chybějící ROS zvýšenou produkcí H2O2. To vyvolá GNG a zpomalí glykolýzu, sníží se také citlivost na inzulín přes dráhu JNK. Malé množství polynenasycených olejů je normální a nezpůsobuje problémy. Při vysokém množství ale ani aktivace PPARα neochrání antioxidační systém v játrech.
Všimněte si na předchozím obrázku, jak PPARα aktivuje inzulinovou rezistenci (P-IRS, citlivost inzulínového receptoru) prostřednictvím doplnění chybějící produkce H2O2 zapojením peroxizomů a následnou reakcí dráhy JNK. Zatímco pro kokosový olej není třeba aktivovat PPARα, což vidíme i na druhém grafu v tomto příspěvku u kyseliny laurové, aktivace transkripčního faktoru PPARα je v přítomnosti polynenasycených olejů naprosto zásadní pro omezení vstupu glukózy a snížení přetížení.
Jak by vypadal metabolizmus polynenasycených tuků bez aktivace PPARα vidíme na následujícím obrázku (modrá křivka).
Ve skutečnosti ale malý obsah PUFA nijak nevadí, naopak produkuje zdravý a hubený fenotyp, jak vidíme na dalším obrázku vlevo. Obsah sojového oleje cca 7 % je asi maximum, které produkuje tento zdravý fenotyp u myší a ještě neničí antioxidační ochranu, neprodukuje 4-HNE, který následně přepne metabolizmus aktivací AR a potlačením SIRT2 a SIRT1. Je možné, že právě omezení exportu VLDL způsobuje tento hubený fenotyp?
Již malé množství linolové kyseliny ve stravě dokáže silně potlačit produkci VLDL a pokud fungují ostatní regulační systémy správně, glukoneogeneze a produkce jaterního glykogenu omezí i příjem potravy. To, myslím, vidíme na následujícím obrázku vlevo. Naopak na obrázku vpravo vidíme, co se stane, když antioxidační ochrana je překonána vysokým množstvím PUFA.
Pokud ještě navíc vezmeme v úvahu, že zvýšení počtu částic VLDL/LDL je nezbytnou součástí imunitní reakce na bakteriální infekci, pak musíme dojít k závěru, že polynenasycené tuky zhoršují naši imunitu v situaci, kdy ji nejvíc potřebujeme. Musíme si dát velký pozor, jaké markery a v jakém čase považujeme za prospěšné nebo škodlivé. Jejich násilné snižování nebo zvyšování může mít nečekané důsledky. Prostě není snadné určit, co je prospěšné a co ne.
Zdroje:








Komentáře
Okomentovat