Epidemie obesity a metabolických poruch je v plném proudu, jen nikdo pořádně neví proč. Když se podíváte na staré filmy nebo fotografie, lidí trochu při těle tam najdete velmi málo, a to i v bohaté společnosti. Lidé jedli, co chtěli. Spotřeba cukru vzrůstala, ale projevovalo se to spíš zkaženými zuby než obezitou. Ale dnes? Myslíte, že to je již vyřešeno? Ale kdež, i přes neustálé sportování a posilování s poměrně vysokým rizikem zranění nebo poškození nějaké části těla, křivka obezity v populaci neustále roste. Kde je příčina?
V poslední době se objevila teorie, že za tím může být tzv. AhR receptor. Tento receptor se zapíná při jídle a vypíná po jídle. Ovšem u obézních lidí se tento receptor už nikdy nevypne. Souvisí to s jedy v našem jídle, např. dioxiny spolehlivě zapínají tento receptor. Pokud vás to zajímá, poslechněte si sérii YouTube videí, kterou vytvořil a stále tvoří Brad Marshall. Možná se na ni podíváme v nějakém příštím příspěvku.
Já se pokusím vysvětlit to, proč a jak buňky inklinují k ukládání tuků, trochu jinak. Jako předem přírodou naprogramovaný proces, který se standardně spouští při dostatečně vysoké hladině inzulinu. Ta totiž signalizuje dostatek nebo spíš přebytek jídla. S jídlem se neplýtvá, proto se přebytek ukládá. Ukážeme si, že je to způsobeno potlačením spalování dlouhých nasycených tuků v mitochondriích (M), takže se zvýší podíl spalování tuků v peroxizomech (P). Ty jsou, zdá se, chemickými továrnami na přeměnu nenasycených tuků na nové, nasycené (Brad Marshall je přirovnává ke skartovačkám všelijakých podivných rozvětvených nenasycených rostlinných tuků - jedů). Navíc právě aktivita peroxizomů potlačuje vstup tuků do mitochondrií. Vysoká hladina inzulinu tedy spustí továrnu na ukládání tuků. To je normální. Co není normální je, když se tuk ukládá i v situaci, kdy je inzulin o dva řády níže, tedy i při relativním nedostatku jídla. Je to vůbec možné? Ano, je.


Podívejte se na grafy výše a porovnejte si na prvním grafu poměr P/M pro hodnotu insulinu -9 (10E-9) tedy 1 nM a pro hodnotu -7 (1E-7) tedy 100 nM. Na horním grafu je rychlost spalování kyseliny palmitové, tedy přibližně rychlost spalování nasycených tuků. Hodnota 1 nM je nízká hladina, hodnota 100 nM je vysoká hladina při jídle. Zajímá nás poměr, nikoli absolutní velikost. Vidíme, že poměr P/M je daleko vyšší při vyšší hladině inzulinu. Je potlačeno spalování tuků v mitochondriích, ale ne při nízké hladině inzulinu. To platí pro dlouhé nasycené tuky běžně obsažené v jídle.
Ovšem na druhém grafu vidíte, že stejného poměru, jako při hodnotě 100 nM lze dosáhnout už při hladině insulinu 1 nM. Jak je to možné? Stačí spalovat polynenasycenou kyselinu arachidonovou omega-6. Mitochondrie totiž nemají moc rády nenasycené tuky a polynenasycené ještě méně. Peroxizomy naopak nenasycené tuky vítají a spalují je přednostně. Také přednostně spalují velmi dlouhé nasycené mastné kyseliny, ale těch není tolik.
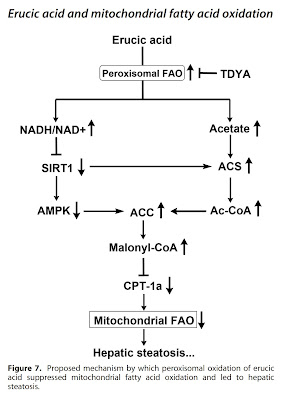
To je celý problém, nadbytek (poly)nenasycených tuků vede ke spalování tuků v peroxizomech už při poměrně nízké hladině inzulinu. To vede k ukládání tuků, protože peroxizomy vypouštějí do buněčného cytosolu suroviny pro výrobu tuků (acetyl-CoA), blokují vstup tuků do mitochondrií (pomocí malonyl-CoA) a navíc zajistí dobrý přístup ke glukóze, která je vpuštěna do buňky zvýšenou produkcí peroxidu vodíku (H2O2). Glukóza je surovinou pro výrobu glycerolu, který váže volně mastné kyseliny do triglyceridů. Ty jsou pak ukládány ve formě tukových kapiček. Navíc glukóza spotřebovaná tělem a uložená do tuku může chybět mozku se všemu možnými důsledky.
No a to je vše, takto olejová kyselina a polynenasycené tuky obsažené ve stolních olejích, přímo ovládají ukládání tuků. Tento proces je v pořádku a umožňuje přežití v přírodě, kdy někdy je dostatek a jindy je nedostatek potravy. A kdy nastanou problémy? Když tato situace trvá příliš dlouho. Peroxizomy totiž produkují poměrně hodně peroxidu vodíku, ten je neutralizován zvýšenou aktivitou glutathion peroxidázy a ta ke své činnosti potřebuje dostatek glutathionu. Ten ovšem časem dojde. A pak teprve nastanou problémy.
Nedostatek glutathionu současně s vysokou aktivitou peroxizomů zvýší hladiny H2O2 a zvýší produkci aldehydů. Navíc i vpustí glukózu do buňky, ta ovšem zpátky nemůže a dopředu nemá kam jít. Vysoká hladina acetátu z peroxizomů způsobí acetylaci enzymů, zejména mitochondriálního komplexu I. Stoupne hladina NADH a NAD+ se stane nedostatkovým. Jediná cesta pro glukózu je otočení reakce laktát dehydrogenázy (LDH) směrem k produkci laktátu. Ten je vypuštěn pryč z buňky, ale až po aktivaci pseudohypoxie (aktivuje se HIF-1α). Aktivita LDH směrem k produkci laktátu zároveň potlačí peroxizomy, ty totiž také přetvářejí pyruvát na laktát, budou si s LDH konkurovat a vzájemně se omezovat. To sníží i produkci H2O2, zvýší hladinu volných mastných kyselina, ještě více aktivuje gluthation peroxidázu a způsobí inzulinovou rezistenci. A nyní víme, proč genetickou deaktivací HIF-1α zabráníme negativním dopadům tučné stravy obsahující polynenasycené tuky. Už jsme to zde probírali. A co dělají MCT oleje?

Tuky se středním řetězcem (MCT) nejsou nijak omezeny aktivitou peroxizomů, mohou vstupovat do mitochondrií bez ohledu na hladinu malonyl-CoA. Mění tedy poměr P/M ve prospěch spalování tuků v mitochondriích a ne směrem k ukládání.
Můžeme si ještě ukázat několik grafů ze studií, ve kterých na zvířecích modelech cíleně zvyšovali (CFB) a snižovali (TDYA) aktivitu peroxizomů pomocí chemických látek při konzumací standardní stravy (N), stravy obohacené o olivový olej (HOO), obohacené o řepkový olej s nízkým obsahem erukové kyseliny (LRO) a řepkový olej s vysokým obsahem erukové kyseliny (HRO). Dnes pěstovaná řepka je vyšlechtěna tak, že obsahuje pouze max. 2 % erukové kyseliny, takže je považována za bezpečnou.
 |
| Srovnání oxidace palmitové nasycené C16 a erukové nenasycené kyseliny C22:1 v játrech potkanů. |
 |
| Zvýšení oxidace v peroxizomech, standardní strava, olivový olej (HOO), řepkový olej (LRO) a eruková kyselina (HRO). |
 |
Zvýšená produkce peroxidu vodíku v peroxizomech, standardní strava, olivový olej (HOO), řepkový olej (LRO) a eruková kyselina (HRO), CFB více aktivuje a TDYA blokuje peroxizomy.
|
 |
| Jaterní tuk, standardní strava, olivový olej (HOO), řepkový olej (LRO) a eruková kyselina (HRO), CFB více aktivuje a TDYA blokuje peroxizomy. |
 |
| Denní přírůstek hmotnosti |
 |
| Zvýšená hladina glukózy při testu infuzí (inzulínová rezistence jako přímý důsledek zvýšené aktivace peroxisomů). |
 |
| Aktivace blokování oxidace tuků v mitochondriích. |
 |
| Potlačení tvorby ketonů, vstup palmitátu je blokován, MCT (octanoate) není blokován. |
 |
| Vliv peroxizomů a složení tuků na oxidaci tuků v mitochondriích. |
 |
| Jaterní ACC je indikátor tvorby tuků. |
 |
| Acetyl-CoA je materiál pro tvorbu tuků. |
 |
| Jaterní SIRT1 indikuje aktivitu deacetylace, tedy odstranění zpomaleného metabolizmu. |
 |
| Aktivace peroxizomů způsobuje nedostatek NAD+ a přebytek NADH (paliva pro oxidaci). |
Malá oprava:První obrázek by měl vypadat takto.
Rozdíl je v tom, že fyziologické hodnoty insulinu jsou o dva řády nižší, než na prvním obrázku. Při půstu (-11) jsou tedy aktivovány více peroxizomy bez ohledu na druh spalovaného tuku. To znamená, že při půstu je aktivován úsporný mechanismus, šetří se uložené tuky i cukry. Věci se změní až při zvýšeném insulinu, při jídle a po něm (-9). Nasycené tuky, jako např. palmitová kyselina C16:0, neaktivuje spalování tuků v peroxizomech, což umožní nerušené spalování tuků v mitochondriích a podpoří výdej energie teplem nebo jinými aktivitami. Nenasycené tuky naproti tomu aktivují spalování v peroxizomech a ponechají je v chodu jako při půstu, potlačí spalování tuků v mitochondriích, tělo zůstane v úsporném režimu a tuky se budou nově tvořit a ukládat.
Navíc spalování v peroxizomech je omezeno hlavně množstvím dostupného NAD+ a tedy dostupností kyslíku. Peroxizomy ale omezují vstup paliva do TCA cyklu, tedy omezují produkci CO2. V tomto příspěvku se dozvíte, jak je důležitý CO2 pro dostatek kyslíku v tkáních. Pokud se podaří zachovat dostatek kyslíku, obnovuje se hladina NAD+ a metabolizmus je zrychlen. Pokud je ho nedostatek, aktivuje se stav hypoxie a metabolizmus je zpomalen. To by vysvětlovalo obrovský vliv správného dýchání nosem, které zadržuje CO2 v těle, na rychlost metabolizmu, zejména při spalování tuků. Nenasycené tuky podporují vznik hypoxie, která nás nutí dýchat více zhluboka nebo ústy a ochuzuje nás o CO2. Toto přirozené chování ještě více ochuzuje tkáně o kyslík a prohlubuje hypoxii tkání, zejména v tukové tkáni.

















Komentáře
Okomentovat