Oxid dusnatý, zásobení tkání kyslíkem a fotobiomodulace, jak to souvisí?
Je zajímavé, jak různorodý pohled na oxid dusnatý (NO) může být. V prvním příspěvku jsem přebíral informace od výzkumníka, který viděl jen samá pozitiva. Ani náznak nějakého vyváženého pohledu, inu hlas prodejce doplňků generujících NO. Tento pohled je dán soustředěním se pouze na jednu funkci NO, totiž vazodilataci. To je sice důležitá funkce, ale není jediná, kterou NO vykonává. Přebytek NO je poměrně destrukční, permanentně modifikuje enzymy a poškozuje funkci např. nervové soustavy, to už jsem také komentoval.
V tomto příspěvku přebírám informace z jednoho článku, který se zabývá zkoumáním fotobiomodulace. Je to poměrně nový obor, kdy tkáň je ozařována buď LED zářením nebo laserem, nebo třeba jen širokospektrálně sluncem nebo žárovkou. Panuje zde řada nejasností a už vůbec nejsou detailně známé mechanizmy, jak to celé probíhá. Jsou známy pozitivní účinky, ale reprodukovatelnost výsledků je problematická právě proto, že se neví, proč to celé funguje.
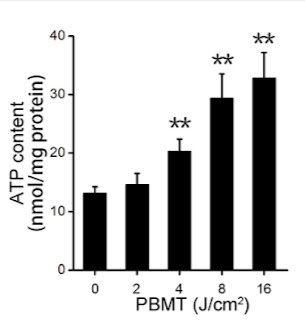
Co umí fotobiomodulace (PBMT), to si ukážeme třeba z této studie na dvou myších modelech diabetu (db/db) a obezity při tučné stravě (HFD). Ozařování dvě hodiny denně dokáže během deseti týdnů napravit krevní cukr a obnovit hladinu ATP, tedy chemické energie pro buňky. Stačí pouze ozářit myši červeným laserovým světlem, v tomto případě o vlnové délce 635 nm. A účinek je přímo úměrný celkové energii dodané laserem.
Mechanismus fotobiomodulace není dosud objasněný. Z výše uvedené studie vyplývá, že ozářením dojde ke zvýšení tvorby superoxidu a peroxidu vodíku, tedy volných radikálů (ROS), toto je nějak zprostředkováno nebo způsobí zvýšení aktivity cytochrom c oxidázy (CcO), tedy čtvrtého mitochondriálního komplexu elektronového transportního řetězce pro získávání energie ATP z našeho jídla. Ale pokud je fotobiomodulační terapie doplněna o antioxidanty, zde použili N-acetyl cystein (NAC), veškerý efekt je anulován. Žádné zlepšení. Potlačení aktivity čtvrtého komplexu (CcO) také vede k vymazání účinků terapie.
 |
| Za účinky fotobiomodulace (PBMT) stojí čtvrtý mitochondriální komplex (CcO). |
Jak to souvisí s oxidem dusnatým? Nejprve se podíváme na to, jak NO ovlivňuje spalování, tedy oxidační fosforylaci, prostřednictvím modulace funkce čtvrtého mitochondriálního komplexu (cytochrom c oxidázy CcO) elektronového transportního řetězce (ETC). Řada vědců se snaží vytvořit matematické modely, které by co nejpřesněji umožňovaly pochopit děje, které se zde odehrávají. Jsou totiž velmi složité a závislé na podmínkách. Je celkem jasné, že NO zde soupeří s kyslíkem a brzdí základní funkci oxidace. Toto zpomalení činnosti je největší při mírném nedostatku kyslíku. Pokud je kyslíku hodně, žádné zpomalení oxidace se nekoná. Nemůžu si pomoci, ale zase je zde centrálním problémem hypoxie. Jak že vzniká? Nedostatkem NAD+, zastaveným TCA cyklem, nedostatečnou produkcí CO2, nedostatkem glutathionu, spalováním tuků při nefunkčním antioxidačním řetězci.
Další funkcí NO je pravděpodobně vazba na hemoglobin nebo myoglobin, NO je vyměněn za uvolněný kyslík a může tedy zajistit více kyslíku pro danou tkáň. Více NO způsobí na jedné straně šetření kyslíkem a zlepší rozvedení kyslíku do celé tkáně, ale zároveň jako prostředek výměny za kyslík může funkčně nahradit chybějící CO2 a zajistit více kyslíku pro tkáň.
 |
| Rychlost oxidace (červeně), tedy aktivita CcO, je výrazně omezena oxidem dusnatým po přidání L-argininu a je obnovena po přidání oxyhemoglobinu HbO2 nebo po osvícení bílým světlem. |
Nejlogičtější se mi tedy zdá vysvětlení, že při nedostatku kyslíku si buňky kyslík rovnoměrně rozdělí mezi sebou. Kyslík se nespotřebuje v první řadě buněk, ale může difundovat i dále. Navíc ještě nějaký ten NO vyrobí z dostupného dusitanu. Skvělá ochrana tkání při nedostatku kyslíku. Pokud při nedostatku kyslíku zajistíme stimulaci červeným světlem, zvýší se tvorba NO z dusitanů pomocí CcO. To nejen šetří kyslík, ale i zajistí předání více kyslíku do tkáně z hemoglobinu nebo myoglobinu. K produkci NO tak stačí ozářit tkáň červenym světlem, nejlépe to pracuje při 590 nm.
Stimulace světlem neboli laserová fotobiomodulace někdy nazývaná low level laser therapy (LLLT) je prostě zajímavá, dokáže zcela reverzovat modulaci činnosti čtvrtého komplexu (CcO) oxidem dusnatým a tedy vrátit spalování na výchozí hodnoty, odstranit inzulinovou rezistenci a celkově napravit metabolizmus. Skoro to vypadá, že právě omezení aktivity CcO oxidem dusnatým je také mechanizmus inzulinové rezistence. A nakonec, i obyčejné červené laserové ukazovátko (650 nm) lze použít jako domácí prostředek pro LLLT.
Zdroje:
Kinetic model of the inhibition of respiration by endogenous nitric oxide in intact cells



Komentáře
Okomentovat